09月22日, 2014 205次
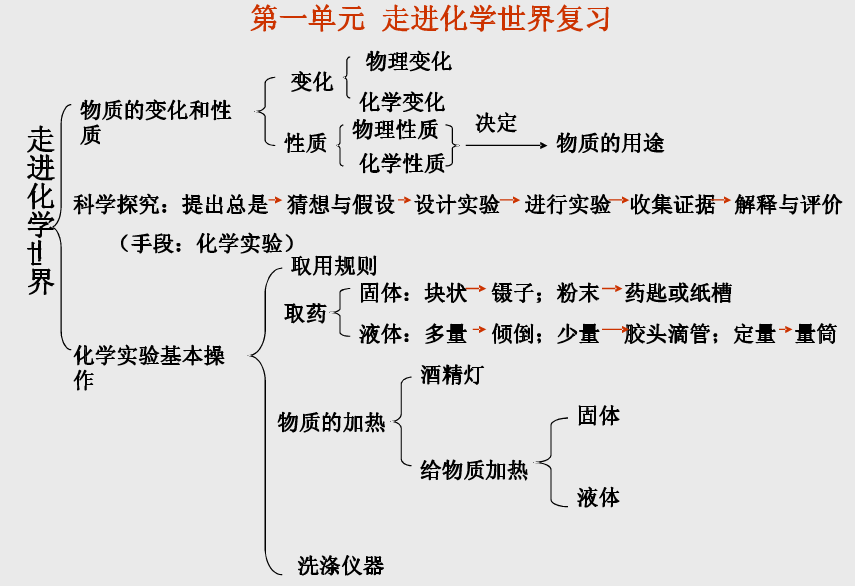
亚原子的构造(九班级化学亚原子的构造常识点整治)
一、亚原子的形成
1、亚原子体积很小,亚原子核更小,亚原子不是实心球
2、亚原子的构造
3、亚原子不带电的因为
由百思特网于亚原子核内质子所带电荷与核外电子的电荷数目十分,电性差异,所以,亚原子不显电性。
4、核电荷数=质子数=核外电子数
5、由表3-1可知
(1)不是一切的亚原子都含有中子。
(2)质子数=核外电子数
(3)同一亚原子中,质子数不确定即是中子数。
(4)各别品种的亚原子核内质子数各别。
二、核外电子排布
1、原百思特网子核外有很大空间,电子在这个空间里作高速疏通
2、核外电子的分层疏通叫作分层排布
3、离核近的电子能量低,离核远的电子能量高
4、核外电子排布顺序
(1)第一层最多包含2个电子,第二层最多包含8个电子,最外层最多包含8个电子(若第一层为最外层时,最多包含2个电子)
(2)排满第一层(2个电子)再排第二层,第二层排满8个电子后,再排第三层(仅限前三层)
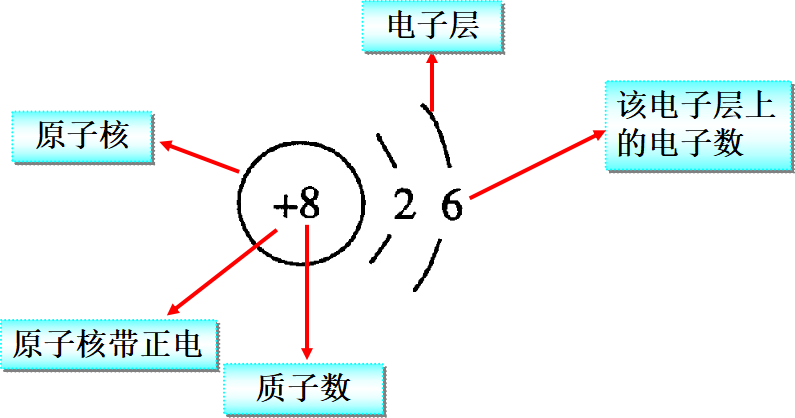
5、亚原子构造表示图

(1)亚原子构造表示图的意旨
6、亚原子百思特网最外层有8个电子(氦为2个电子)的构造是对立宁静构造
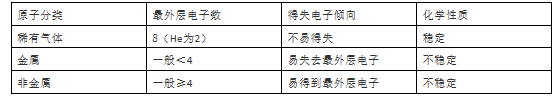
7、亚原子品种与亚原子构造的联系
8、亚原子的最外层电子数确定亚原子的化学本质。
9、普遍情景下,最外层电子数沟通的亚原子具备一致的化学本质;惯例:氦(He)和镁(Mg)最外层电子数沟通,化学本质不一致